“一物一碼”技術應用在醫療器械行業,就是醫療器械唯一標識UDI,其目的是建立醫療器械產品全生命周期監管體系,加強對醫械產品的質量監督。
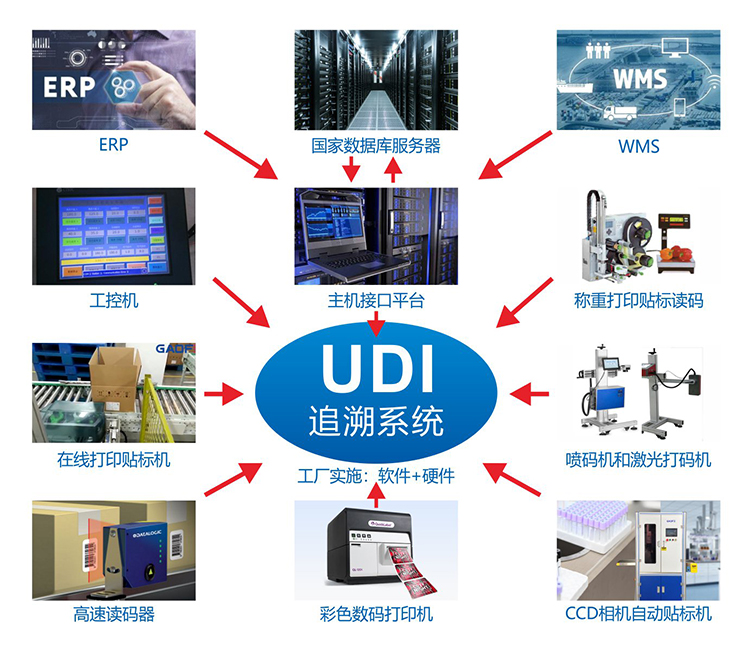
完整的UDI系統包括UDI編碼、UDI數據載體和數據庫: UDI編碼是一串全球唯一的代碼,是醫療器械的數字“身份證”。 UDI數據載體是UDI編碼的表現形式,如一維碼、二維碼等。 UDI數據庫是儲存UDI編碼信息的數據庫。 三者共同構成U D I體系。
 近年來,UDI在世界各國迅速推廣,中國、美國、歐盟、日韓等國家和地區紛紛要求在本國銷售、流通的醫療器械必須具備UDI。本期先來聊聊UDI的國際發展情況。
近年來,UDI在世界各國迅速推廣,中國、美國、歐盟、日韓等國家和地區紛紛要求在本國銷售、流通的醫療器械必須具備UDI。本期先來聊聊UDI的國際發展情況。
2011年國際醫療器械監管機構論壇(IMDRF)成立,2013年12月發布《UDI指南》、2019年3月發布《醫療器械唯一標識系統應用指南》,為建立全球互認的UDI系統提供了技術框架。
美國早在2007年《FDA修正案》就正式確立了實施UDI的立法依據。2012年7月發布《UDI法規提案》,2013年9月發布《UDI最終法規》,計劃用7年時間對不同醫療器械產品分階段推進并逐步實施UDI管理。 目前,美國已基本實現所有醫療器械產品的UDI覆蓋。這也意味著,出口美國的各類醫療器械全部需要實施UDI。
歐盟在2013年4月發布《UDI系統通用框架的指導意見》,2017年5月發布《醫療器械法規》(MDR),對醫療器械基于UDI的追溯管理提出要求,并計劃分階段實施UDI。 隨后,歐盟數據庫逐步完善各功能板塊并開放注冊,2022年5月26日,數據庫開放UDI板塊,要求MDR的Ⅲ類產品申報DI。2023年5月26日,實施范圍擴大到了MDR的Ⅱa、Ⅱb、Ⅲ類-可重復使用產品、IVD的Class D產品。
日本厚生省于2018年3月發布通知《醫療器械標識代碼放置指南》,用3年按照風險等級逐步推進,并建立了國家數據庫。
韓國已完成了各類醫療器械的合規進程。出口韓國的各類醫療器械都需要完成UDI實施。
沙特阿拉伯要求在2023年9月1日前,D類(高風險)、B/C類(中等風險)需要完成UDI合規。
中國臺灣要求,截止日期2023年6月,Ⅱ類醫療器械需要完成UDI合規。
除以上國家或地區外,越來越多的國家或地區也陸續發布了UDI相關法規。



